【一区家族】灰飞虱UGT基因家族分析
一、文章基本信息
发表时间:2025 年 6 月 17 日
第一单位:山东省农业科学院经济作物研究所(Institute of Industrial Crops, Shandong Academy of Agricultural Sciences)
通讯作者:(Jianhua Zhang),邮箱:zhangjianhua198904@163.com
发表题目:Contribution of UDP-glycosyltransferases to triflumezopyrim tolerance regulated by microRNAs in Laodelphax striatellus
发表期刊:《农药生物化学与生理学》(Pesticide Biochemistry and Physiology) DOI:

二、摘要
高效的解毒能力是害虫在杀虫剂选择压力下存活的关键。UDP-糖基转移酶(UGT)作为Ⅱ相解毒酶超家族,可催化多种疏水性外源化合物与糖基结合形成水溶性糖苷并排出体外。微小RNA(miRNA)作为重要的转录后调控因子,可通过靶向解毒酶基因参与杀虫剂抗性形成。
本研究在灰飞虱(SBPH,Laodelphax striatellus)基因组鉴定出 21 个 UGT 基因,其中 16 个属于 UGT386 家族,提示该家族存在显著扩张。LD50 剂量的三氟苯嘧啶处理后,UGT 活性升高 2.09 倍;协同剂试验证实 UGT 参与耐受。UGT386G1 与 UGT386J1 表达上调 >2 倍,RNAi 仅抑制这两个基因即可显著增加灰飞虱对三氟苯嘧啶的敏感性。生物信息学预测并实验验证 miR-281-5p 和 PC-3p-4042_506 分别通过结合 UGT386G1 与 UGT386J1 的 CDS 区实现转录后负调控;agomir 过表达及双荧光素酶报告试验均证实该调控关系。
研究首次揭示 miRNA-UGT 模块介导灰飞虱对三氟苯嘧啶的耐受机制,为延缓该新型杀虫剂抗性发展提供理论依据与潜在分子靶点。
三、主要内容
图1
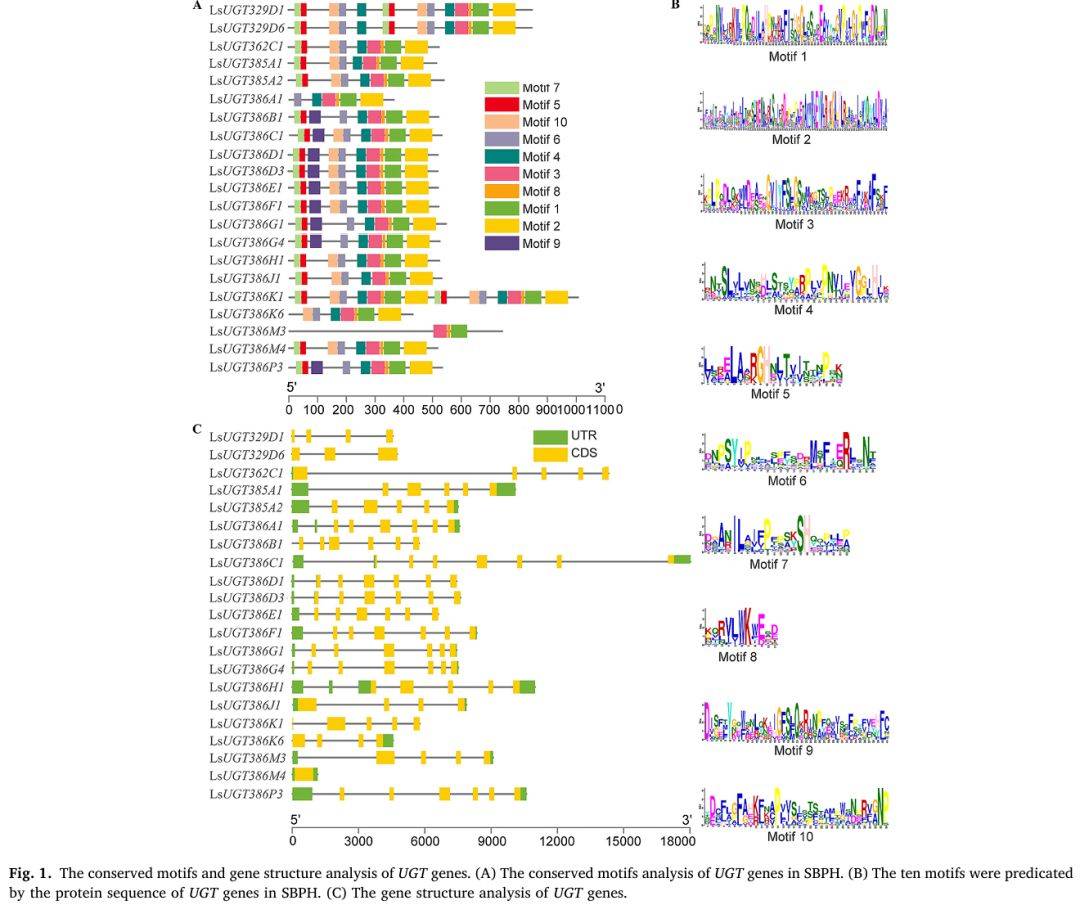
作者在灰飞虱(SBPH)基因组中共鉴定到 21 个 UGT 基因,其中 16 个属于 UGT386 家族,提示该家族存在显著扩张。利用 MEME 软件对蛋白序列进行保守基序分析,发现同一亚家族成员具有高度相似的基序排列;基因结构分析显示外显子数目 1–6 个不等,且同一亚家族内含子/外显子格局趋于一致。染色体定位表明 21 个基因不均匀分布于 7 条染色体,chr.8 与 chr.9 分别含有 6 个与 5 个基因,共线性分析进一步揭示 11 对片段重复事件,说明基因复制是 UGT386 家族扩张的主要驱动力。
展开全文
图例说明:灰飞虱 UGT 基因的保守基序与基因结构分析
A) 21 个 UGT 蛋白的保守基序(Motif 1–10)排列图,同一亚家族基序组成高度相似。
B) 10 个基序的序列标识与长度(11–80 aa),用于功能结构域推断。
C) 基因结构图:外显子-内含子分布,显示 UGT386 亚家族内含子数目变异小,结构保守。

图2
为阐明 UGT 基因在染色体上的分布与进化关系,作者绘制了 SBPH 全部 UGT 的染色体定位图,并与其近缘种褐飞虱(BPH)进行共线性比对。结果显示 21 个基因散布于 7 条染色体,chr.8 与 chr.9 为两大热点区域;MCScanX 共线性分析发现 11 对片段重复(红线),提示片段复制驱动家族扩张;跨物种共线性显示 SBPH 与 BPH 间存在 9 对直系同源 UGT 基因(红线),表明这些基因在两类稻飞虱中功能可能保守。
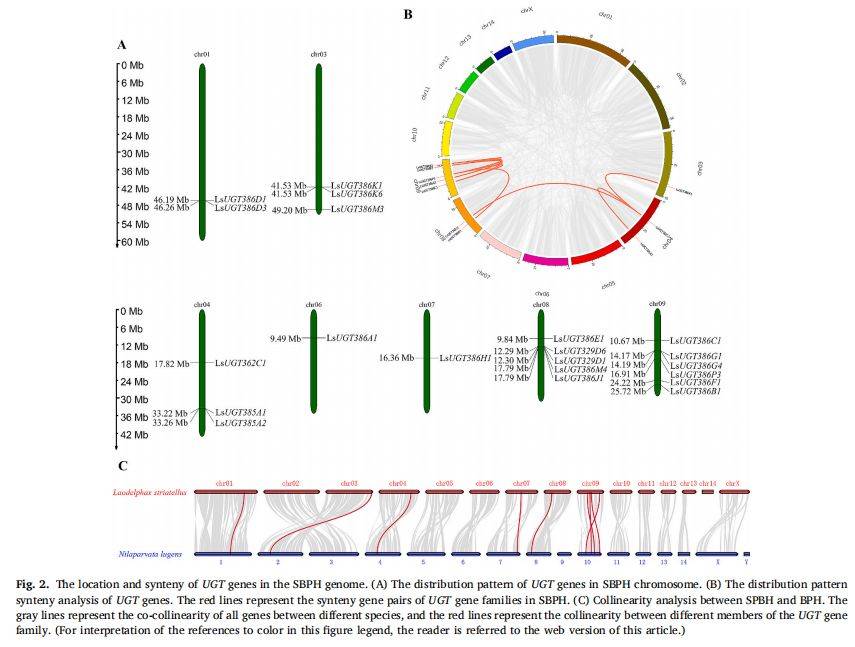
图例说明:灰飞虱基因组中 UGT 基因的染色体定位与共线性关系
A) 染色体定位图:每条染色体上 UGT 基因位置(Mb 刻度),颜色区分不同亚家族。
B) 片段重复图:红线连接 SBPH 内部 11 对共线 UGT 基因,揭示片段复制事件。
C) 跨物种共线性:灰线示全基因组共线,红线突出 SBPH 与 BPH 间 9 对直系同源 UGT 基因。

图3
通过测定 α-萘酚为底物的 UGT 酶活性,作者发现 LD50 剂量三氟苯嘧啶处理后酶活性提高 2.09 倍;协同剂试验显示 UGT 抑制剂 Sul 与 5-Nul 分别使死亡率由 47.98 % 升至 63.5 % 与 59.57 %,证实 UGT 参与解毒。 qRT-PCR 筛选出 9 个显著上调基因,其中 UGT385A1、UGT386G1 与 UGT386J1 上调 >2 倍;dsRNA 干扰显示仅 UGT386G1 与 UGT386J1 敲低可显著增加灰飞虱对药剂敏感性(死亡率由 44 % 升至 72 % 与 69 %),且二者在中肠与脂肪体高表达,提示其为耐受关键基因。
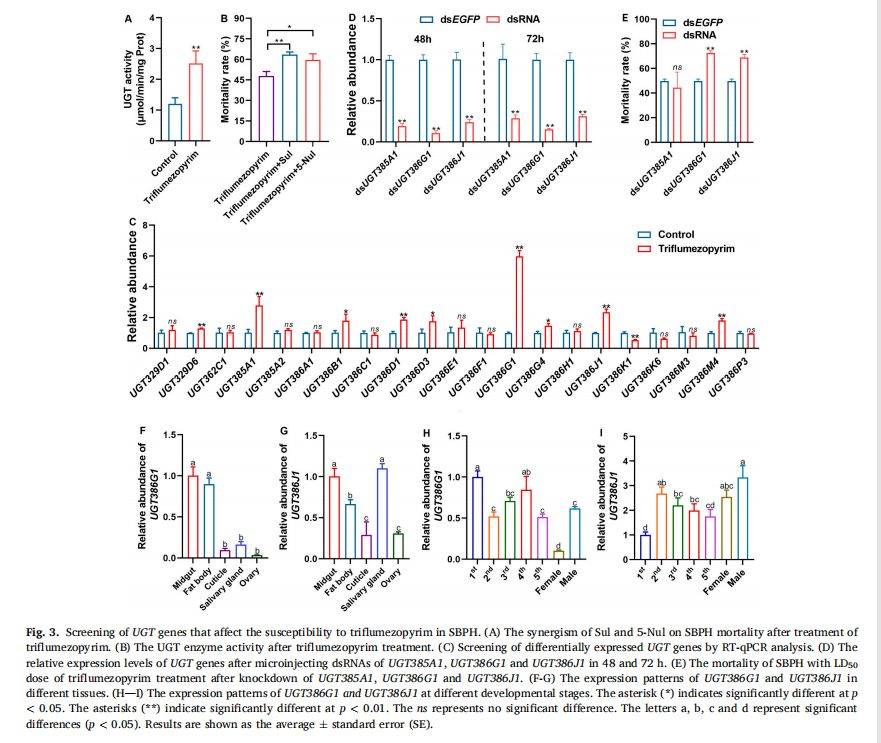
图例说明:影响灰飞虱对三氟苯嘧啶敏感性差异的 UGT 基因筛选
A) 协同剂试验:Sul 与 5-Nul 显著提高三氟苯嘧啶死亡率(48 h)。
B) 酶活性测定:药剂组 UGT 活性为对照 2.09 倍。
C) qRT-PCR 筛选:21 个基因表达热图,9 个上调,3 个 >2 倍。
D) RNAi 效率:dsRNA 48/72 h 后靶基因表达下降 >50 %。
E) 死亡率统计:UGT386G1/J1 干扰后死亡率显著升高。
F-G) 组织表达谱:中肠、脂肪体高表达,UGT386J1 在唾液腺最高。
H-I) 发育表达谱:UGT386G1 若虫期高,UGT386J1 雄成虫最高。

图4
利用 TargetScan 与 miRanda 预测并 qRT-PCR 验证,作者发现 miR-281-5p、miR-10-3p 与 PC-3p-4042506 可靶向 UGT386G1,PC-3p-4042506 与 miR-750-3p 可靶向 UGT386J1。药剂处理后上述 miRNA 表达显著下调;agomir 过表达实验显示仅 miR-281-5p 可使 UGT386G1 表达下降 85 %,PC-3p-4042_506 使 UGT386J1 下降 55 %,并显著提高灰飞虱对药剂敏感性(死亡率由 46 % 提升至 58 % 与 55 %)。组织与发育表达谱显示两 miRNA 在唾液腺及雄成虫高表达,与靶基因呈负相关,提示其参与转录后调控。
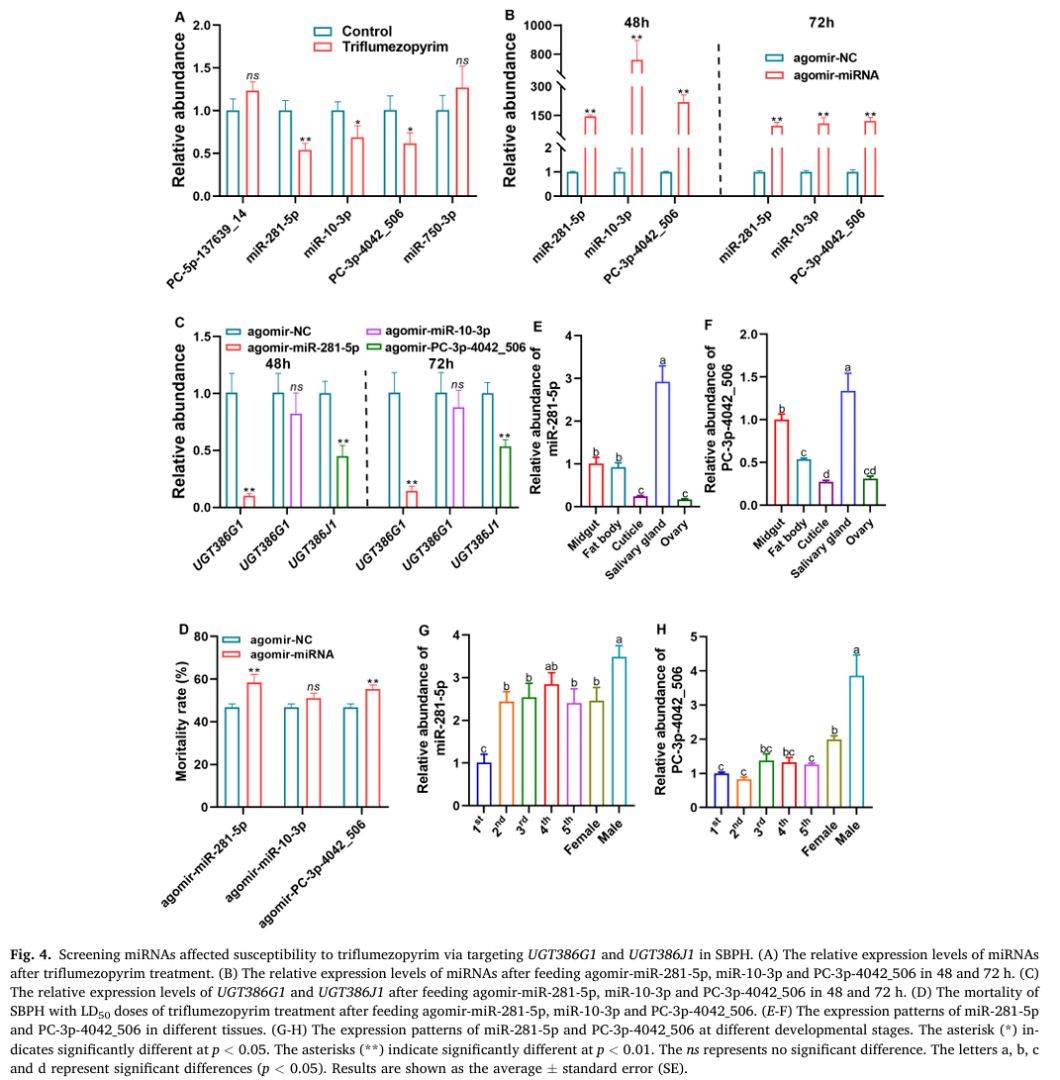
图例说明:通过靶向 UGT386G1 与 UGT386J1 进而影响灰飞虱对三氟苯嘧啶敏感性的 miRNA 筛选
A) 药剂处理后 5 个预测 miRNA 表达变化。
B) agomir 注射后 miRNA 表达升高 >90 倍。
C) agomir 注射后靶基因表达:miR-281-5p 使 UGT386G1 下降 85 %,PC-3p-4042_506 使 UGT386J1 下降 55 %。
D) 死亡率测定:两 miRNA 过表达显著增加药剂致死率。
E-F) 组织表达谱:唾液腺高表达,与靶基因负相关。
G-H) 发育表达谱:雄成虫表达峰值,与靶基因趋势相反。

图5
为验证 miRNA 与靶基因的直接互作,作者将 UGT386G1 与 UGT386J1 的 CDS 野生型及突变体序列克隆至 pmirGLO 双荧光素酶报告载体,并与对应 miRNA mimics 共转染 HEK293T 细胞。结果显示:miR-281-5p 可使野生型 UGT386G1 荧光素酶活性降至 65.3 %,PC-3p-4042_506 使野生型 UGT386J1 活性降至 69.9 %;而靶位点突变后抑制效应消失,证实两 miRNA 分别通过结合 CDS 区实现对 UGT 基因的转录后负调控。
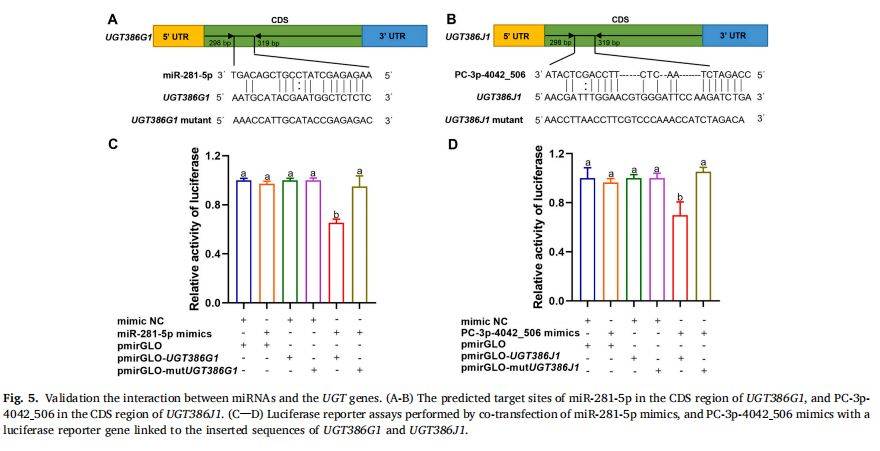
图例说明:miRNA 与 UGT 基因相互作用的验证(双荧光素酶报告试验)
A-B) 靶位点示意图:miR-281-5p 与 UGT386G1 CDS、PC-3p-4042_506 与 UGT386J1 CDS 结合序列及突变设计。
C-D) 双荧光素酶报告试验:野生型载体+miRNA mimics 荧光素酶活性显著下降,突变型无抑制,P<0.01。

图6
作者综合上述结果绘制模式图,清晰展示“三氟苯嘧啶处理 → miR-281-5p/PC-3p-4042_506 表达下调 → UGT386G1/UGT386J1 去抑制上调 → 酶活性增强 → 杀虫剂糖基化代谢加速 → 灰飞虱耐受性提高”的完整调控链。该图强调 miRNA 位于信号起点,通过转录后去抑制机制快速放大 UGT 介导的解毒通量,为解释新杀虫剂耐受性形成提供简洁直观的分子模型 。
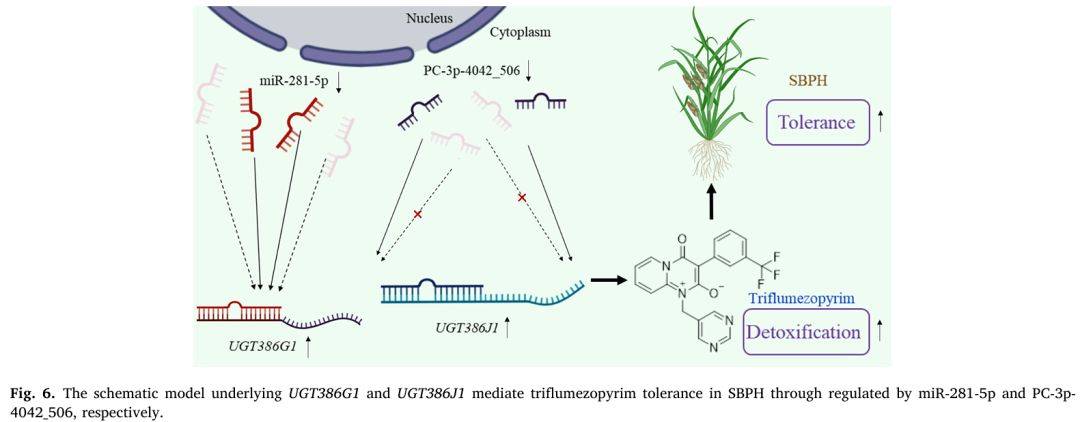
图例说明:miR-281-5p 与 PC-3p-4042_506 调控 UGT386G1 和 UGT386J1 介导灰飞虱对三氟苯嘧啶耐受的模式图
模式图:从药剂刺激、miRNA 下调、UGT 去抑制、解毒增强、耐受性提升五个步骤,完整呈现 miRNA-UGT-耐受 调控轴。
四、总结此文
作者系统鉴定灰飞虱 21 个 UGT 基因,发现 UGT386 家族显著扩张;三氟苯嘧啶诱导 UGT386G1/UGT386J1 高表达,RNAi 证实二者为耐受关键酶。进一步筛选并验证 miR-281-5p 与 PC-3p-4042_506 分别负调控上述 UGT,形成“杀虫剂→miRNA↓→UGT↑→耐受”通路。该研究阐明 miRNA 转录后调控 UGT 参与新杀虫剂解毒的分子机制,为抗性监测与 RNA 干扰治理策略提供新思路。
五、生成思维导图(文字版)
miRNA-UGT 模块介导灰飞虱对三氟苯嘧啶的耐受
背景与目的
三氟苯嘧啶:新型 mesoionic 杀虫剂,高效低毒
亟需揭示耐受机制以延缓抗性
实验设计
基因组鉴定:21 UGTs,UGT386 家族扩张
酶活+协同剂:证实 UGT 参与解毒
RNAi:锁定 UGT386G1/J1 为关键基因
miRNA 预测:筛选 miR-281-5p / PC-3p-4042_506
agomir 过表达:验证 miRNA 负调控 UGT
双荧光素酶:确认靶向 CDS 区
主要结果
UGT 活性↑2.09 倍;协同剂↑死亡率
UGT386G1/J1 表达↑>2 倍;RNAi↑死亡率至 70%
miRNA 过表达→UGT 下调→死亡率↑
靶向关系通过报告基因证实
结论与意义
首次揭示 miRNA-UGT 通路介导三氟苯嘧啶耐受
提供 RNA 干扰或小分子调控的抗性治理新靶点
展望
田间种群验证
开发 miRNA/UGT 双靶点干预策略







评论